La farmacéutica estadounidense anunció que solicitó oficialmente la aprobación de su vacuna contra el COVID-19 para su “uso de emergencia” en niños.
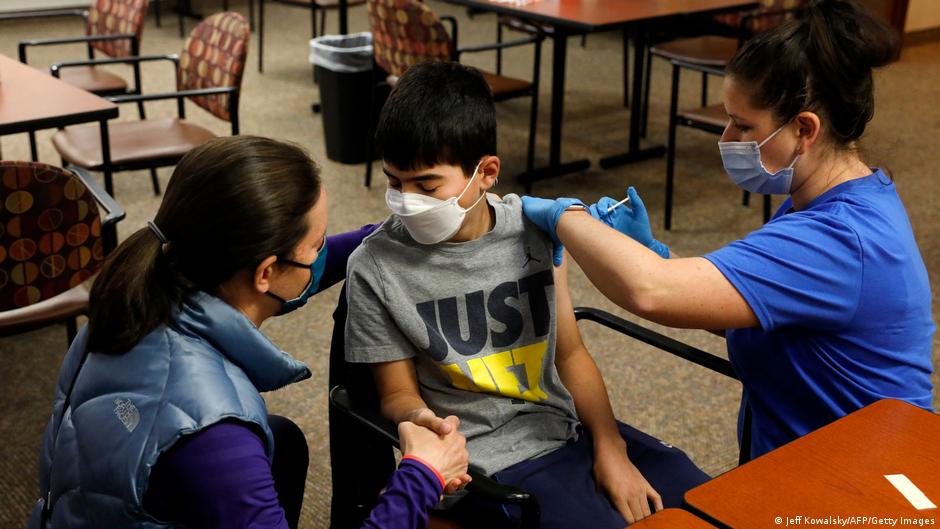
La farmacéutica estadounidense Pfizer anunció este jueves (07.10.2021) que solicitó formalmente a la agencia reguladora en Estados Unidos la autorización de emergencia para administrar su vacuna contra el COVID-19 a niños de entre 5 y 11 años. Los organismos reguladores -la FDA y los Centros de Control de Enfermedades (CDC)- deberán revisar la petición antes de darle luz verde.
Pfizer anunció hoy en Twitter que, junto a la alemana BioNTech, “oficialmente presentaron su pedido a la FDA” para el “uso de emergencia” de la vacuna en niños de 5 a 11 años. A fines de septiembre, ambas empresas, que desarrollaron juntas la vacuna, comenzaron a enviar datos a la agencia FDA, que supervisa en Estados Unidos los medicamentos, para su autorización.
Tras el anuncio, el coordinador de la Casa Blanca para la pandemia, Jeff Zients, dijo a la cadena CNN que “todos estamos de acuerdo en que contar con una vacuna segura y efectiva para chicos de hasta 11 años es el próximo paso realmente importante en la lucha contra el virus”. En el país, muchos menores se han contagiado de la variante delta del virus e inmunizar a los menores se considera clave para mantener abiertas las escuelas y terminar con la pandemia.
En los ensayos, niños de entre 5 y 11 recibieron dos dosis de 10 microgramos con 21 de diferencia entre ambas. Las dos para grupos etarios mayores sobre de 30 microgramos. Las farmacéuticas anunciaron hace diez días que las últimas pruebas clínicas han generado una “robusta” respuesta de anticuerpos y que la vacuna es segura.
La vacuna de Pfizer-BioNTech cuenta con la plena autorización de la FDA para los mayores de 16 años y con la autorización de emergencia para los mayores de 12. La pasada semana, el cirujano general de EE. UU. (el principal responsable de la salud pública del país), Vivek Murthy, aseguró que las vacunas para los niños entre cinco y once años “están ya en el horizonte”.
Las farmacéuticas Pfizer y BioNTech anunciaron hace diez días que los resultados de las últimas pruebas clínicas han generado una “robusta” respuesta de anticuerpos y que la vacuna es segura, lo que acerca la posibilidad de un suero infantil disponible para finales de octubre o principios de noviembre.
lgc (efe/afp)
Fuente: Deutsche Welle